수젠텍, SD바이오센서, 피씨엘, 젠바디, 나노엔텍 등의 신종 코로나바이러스 감염증(코로나19) 항체진단키트가 미국 내 배포리스트에서 삭제됐다.
미국 식품의약국(FDA)의 21일(현지시간) 공지에 따르면 이들 업체는 정책 변경 지침에 따른 긴급사용승인(EUA) 요청이 적절한 시간 내 해결되지 않는 등의 이유로 미국 내 코로나19 진단키트 배포가 금지됐다.
https://www.sedaily.com/NewsView/1Z6OWOR9L3
국산 항체기반 코로나19 진단키트, FDA 배포리스트서 삭제
지난 13일 부산 해운대구 부산기계공고 학생 3명이 확진 판정을 받자 교직원들이 진단검사를 받고 있다. /연합뉴스수젠텍, SD바이오센서, 피씨엘, 젠바디, 나노엔텍 등의 신종 코로나바이러스 감�
www.sedaily.com
코로나 발생 초기에는 항체 진단키트는 FDA승인없이도 등록만 되면 판매가 가능했었다. 하지만 불량 진단키트가 다수 발생함에 따라 EUA 승인을 획득해야 판매할 수 있도록 바뀌었다.
오늘 기사에난 업체들은 FDA에서 항체 진단키트에 대해 EUA 승인을 받으라고 하였고 EUA에서 키트들을 테스트할 결과가 진단키트로써 부적합 판정을 받아서 배포리스트에서 삭제된 것으로 추정된다.
앞으로 EUA승인을 획득할 항체진단키트의 경쟁자가 더 줄어들게 되었다.
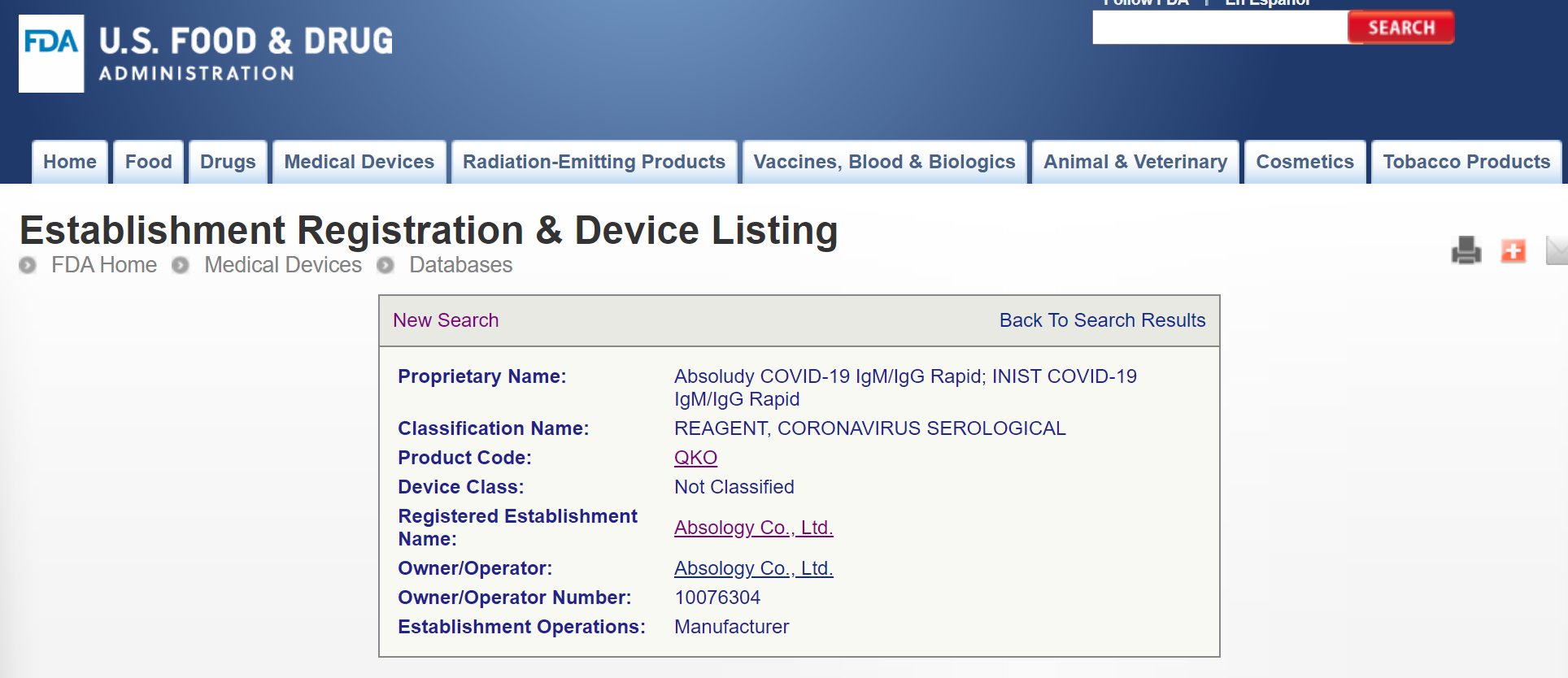
인텍플러스(앱솔로지)의 항체진단키트의 행보가 더더욱 주목된다.
이제 8월도 얼마남지 않았다. 영업일로 치면 6일 남았다. 6일 내에 앱솔로지의 EUA 획득 소식을 기다려본다.
2020/08/09 - [주식/기업] - 인텍플러스, 코로나 진단키트 수혜주로 폭등 기대
2020/08/20 - [주식/기업] - 제2의 엑세스바이오를 노리는 #앱솔로지 feat. #인텍플러스
'주식 > 기업' 카테고리의 다른 글
| #인텍플러스, 2020년 8월 26일 IR 리뷰 (0) | 2020.08.26 |
|---|---|
| #인텍플러스, 기업설명회(IR) 개최 (0) | 2020.08.25 |
| 제2의 엑세스바이오를 노리는 #앱솔로지 feat. #인텍플러스 (0) | 2020.08.20 |
| #엘앤케이바이오, 공장증축의 배경은 수요 증대! (0) | 2020.08.20 |
| #엘앤케이바이오, 높이 조절이 가능한 척추 유합케이지 특허 취득 (0) | 2020.08.18 |