알테오젠 홈페이지에 JP모건 헬스케어 컨퍼런스에 참석한다는 공지가 올라왔다. JP모건 헬스케어 컨퍼런스는 1월 10일부터 13일간 샌프란시스코에서 개최한다.
내용인즉, 이번 컨퍼런스에서 ALT-B4 L/O과 ALT-L9판권 계약과 관련된 미팅을 진행한다는 것이다.
주주 여러분께,
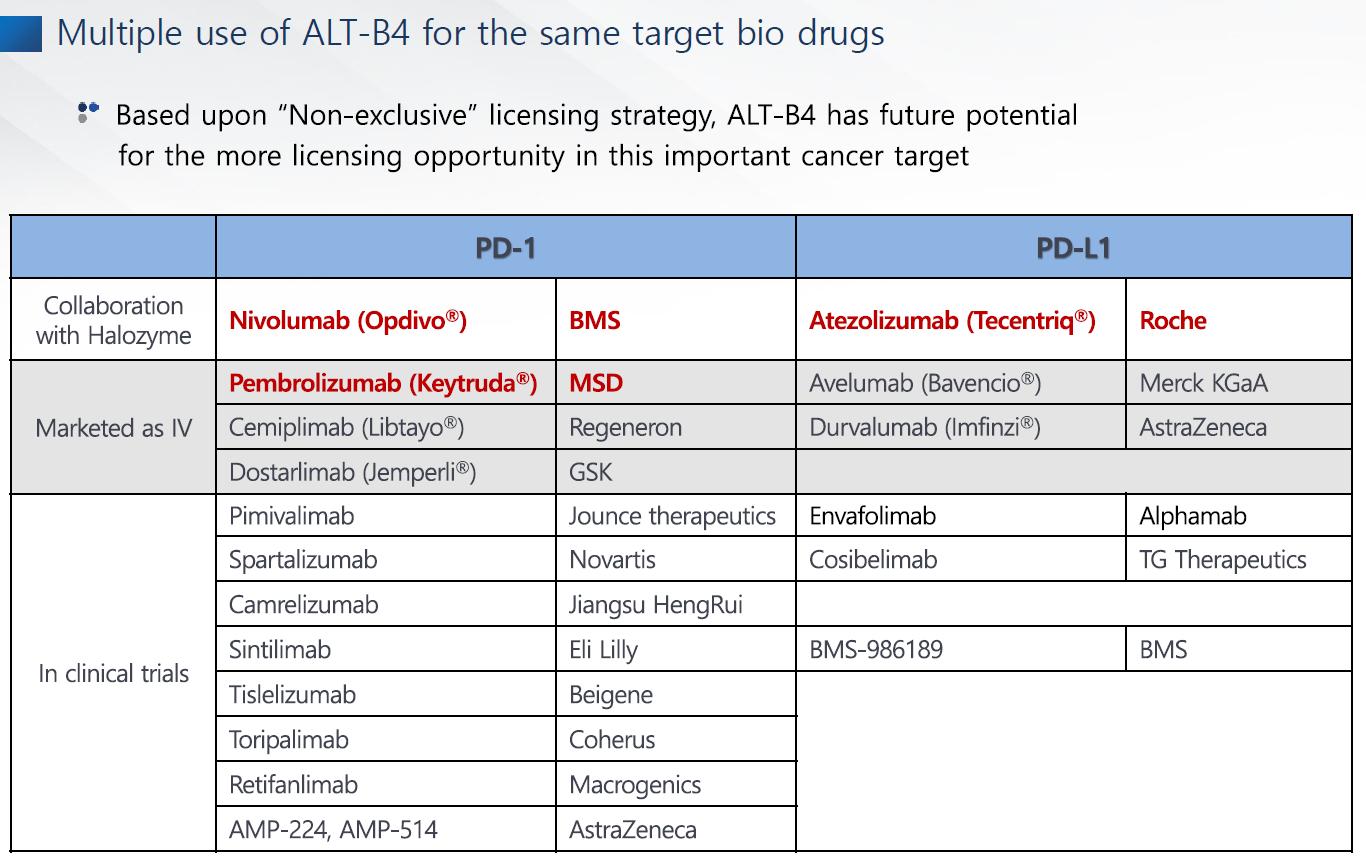
온라인으로 진행되는 이번 JP모건 헬스케어 컨퍼런스에서 행사에서 2020년에 계약한 글로벌 10대 제약사가 최근 임상 1상에 착수한 이래로 다수의 글로벌 제약사들로부터 "ALT-B4"(히알루로니다제)의 품질 및 효력을 인정받고 있음을 실감하고 있습니다.
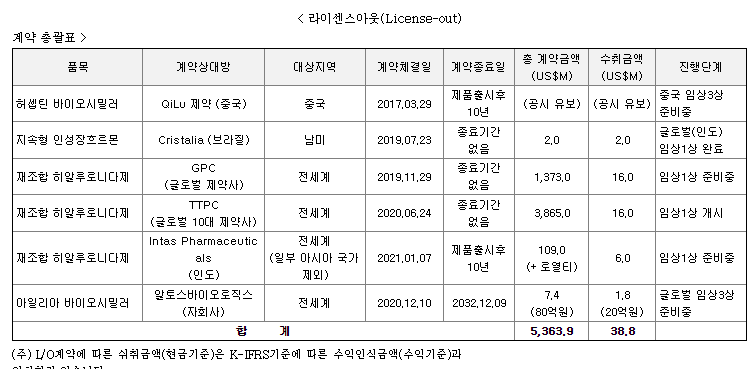
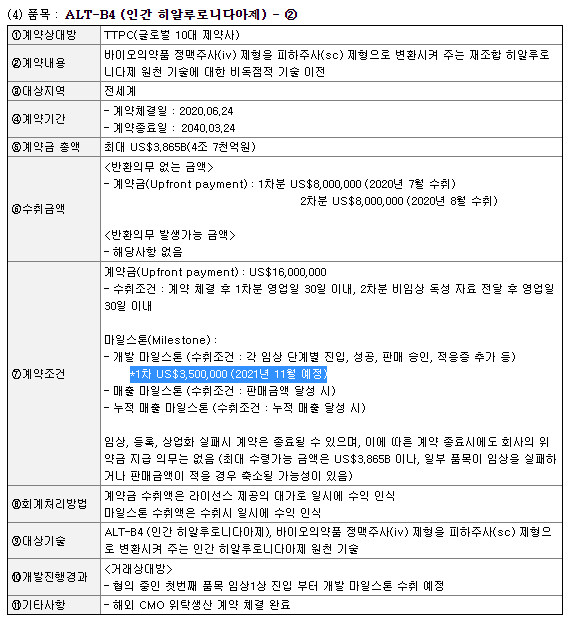
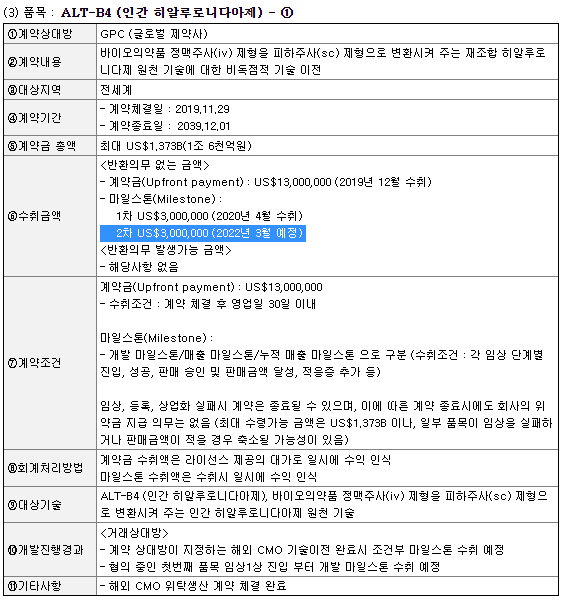
이에 당사는 최근 글로벌 10대 제약사 4곳과 비밀유지협약(CDA) 및 물질이전계약(MTA)을 체결한 이후 기술수출 계약(라이센스아웃) 관련하여 추가적인 협의를 할 예정입니다.
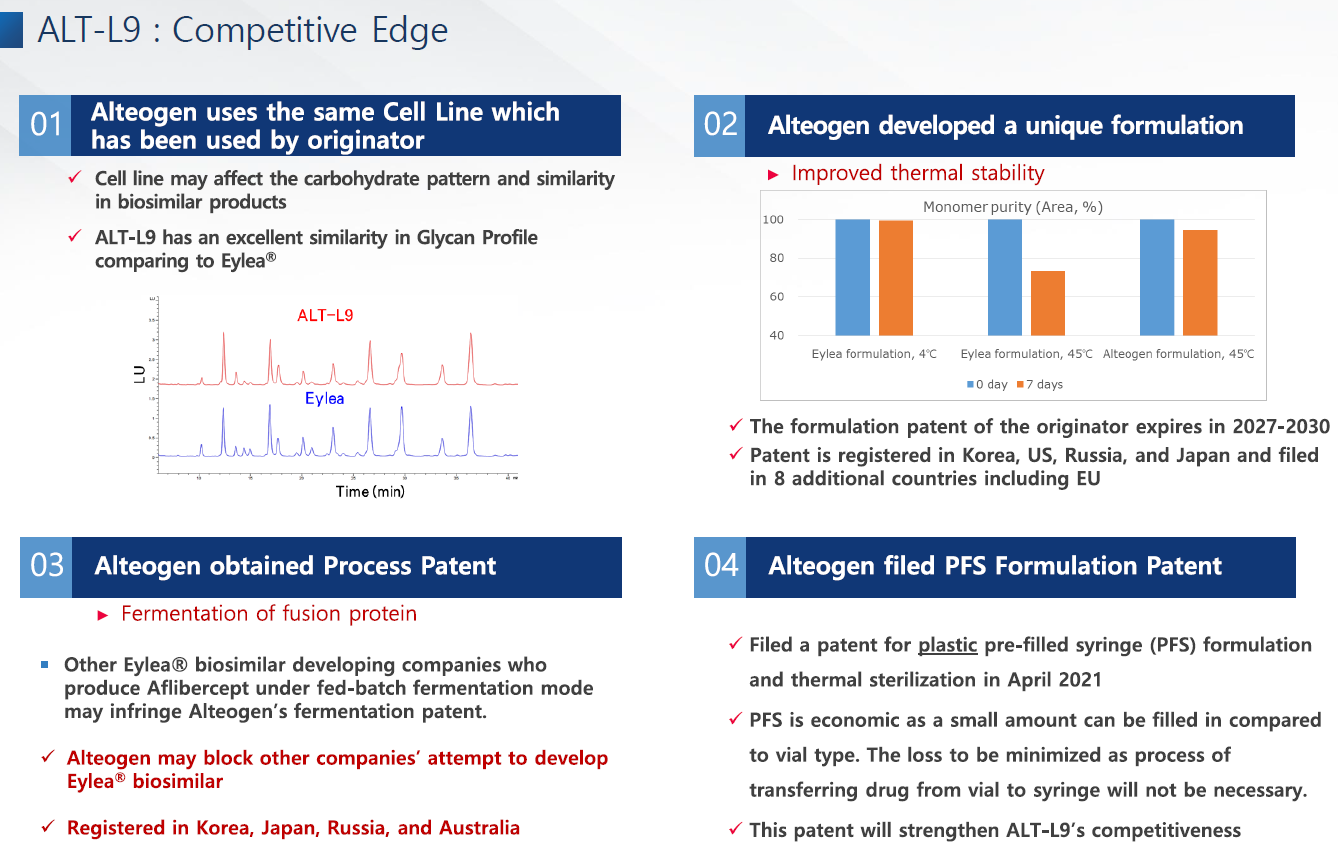
별도로 아일리아 바이오시밀러 "ALT-L9"의 해외 마케팅 계약을 위한 글로벌 제약사들과의 온라인 미팅도 예정되어 있습니다.
주주 여러분들의 지속적인 성원과 관심에 감사 드립니다.
ALT-L9은 지난달에 노이즈가 좀 있었다.
작년 IR에서 박순재 대표가 ALT-L9판권 가능성을 시사했고, 현대차증권 리포트에서는 연내 체결가능성이 있다고 했다.
그래서 주가가 상승하다가 계약이 불발되었다는 찌라시로 인해 주가가 급락하는 사건이 있었다.
결론적으로 보면, 찌라시는 사실이었던 셈이다.
그 후 나온 1월 주주레터를 보면 아래와 같은 구체적인 내용이 있다.
아래 내용으로 추측해서, ALT-L9 사건을 재구성해보면 다음과 같다.
- 글로벌업체A와 ALT-L9 판권 계약 실제하려고 추진 중이었음
- 다른 글로벌업체B,C 등이 다른 조건을 제시하며 등장
- 알테오젠은 A와 계약에 관한 조건만 생각하다가 B와 C가 등장하여 새로운 조건을 제시하니 전반적으로 어떤 계약이 유리한 것인가에 대해 검토해볼 필요성이 생김
- A와 계약 연기

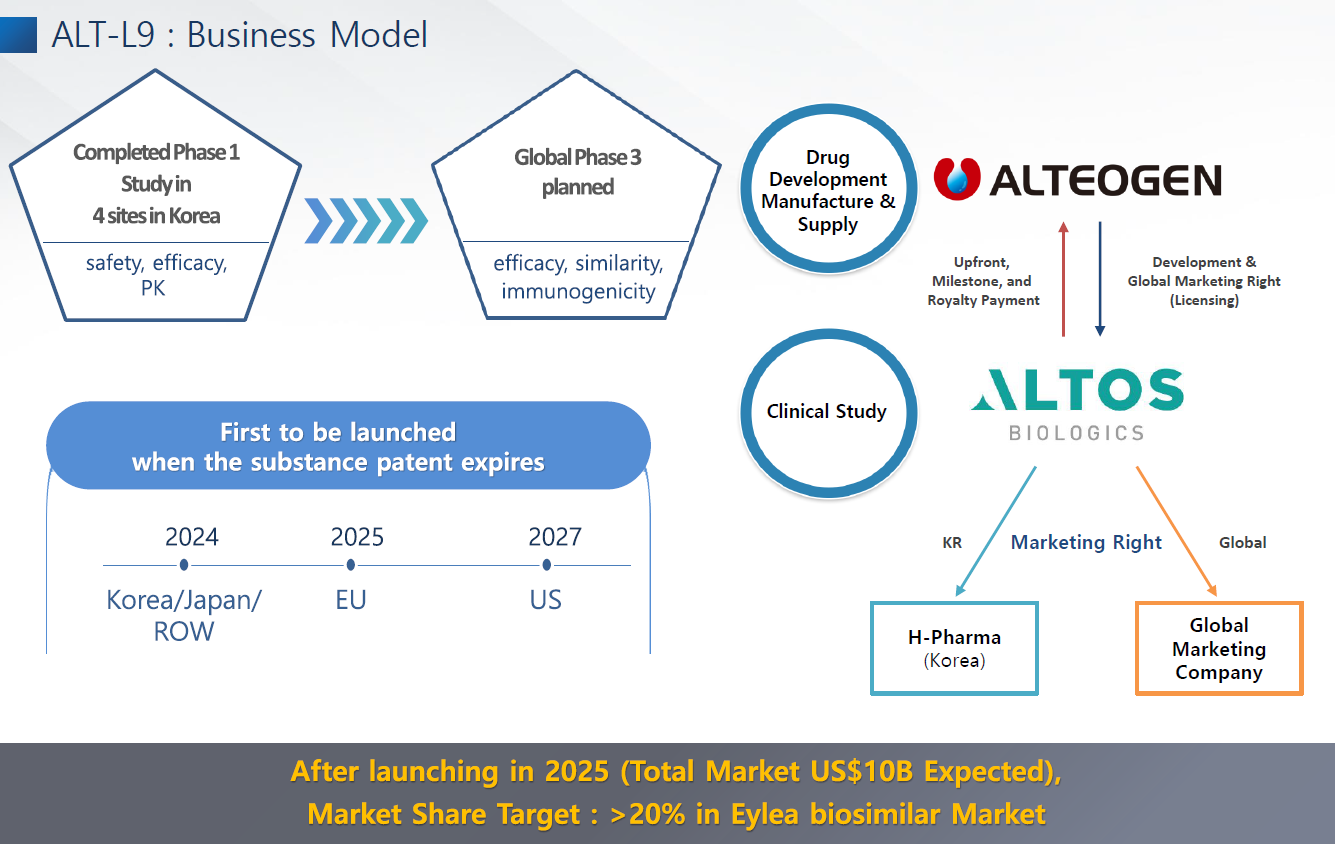
ALT-L9 판권 계약 조건은 크게 보면 2가지다.
- 한 업체와 글로벌 계약
- 지역별로 마케팅 능력이 뛰어난 회사와 계약
최근 기사를 보면, "ALT-L9의 경우 현재 각 지역별로 판권 도입을 희망하는 업체들이 많아 보다 회사에 유리한 조건으로 계약하기 위한 논의가 진행 중이다"라는 문구가 눈에 띈다.
즉, 알테오젠은 지역별(유럽, 미국, 아시아 등)으로 판권을 분리하여 판매하려고 하는 것으로 추정된다.
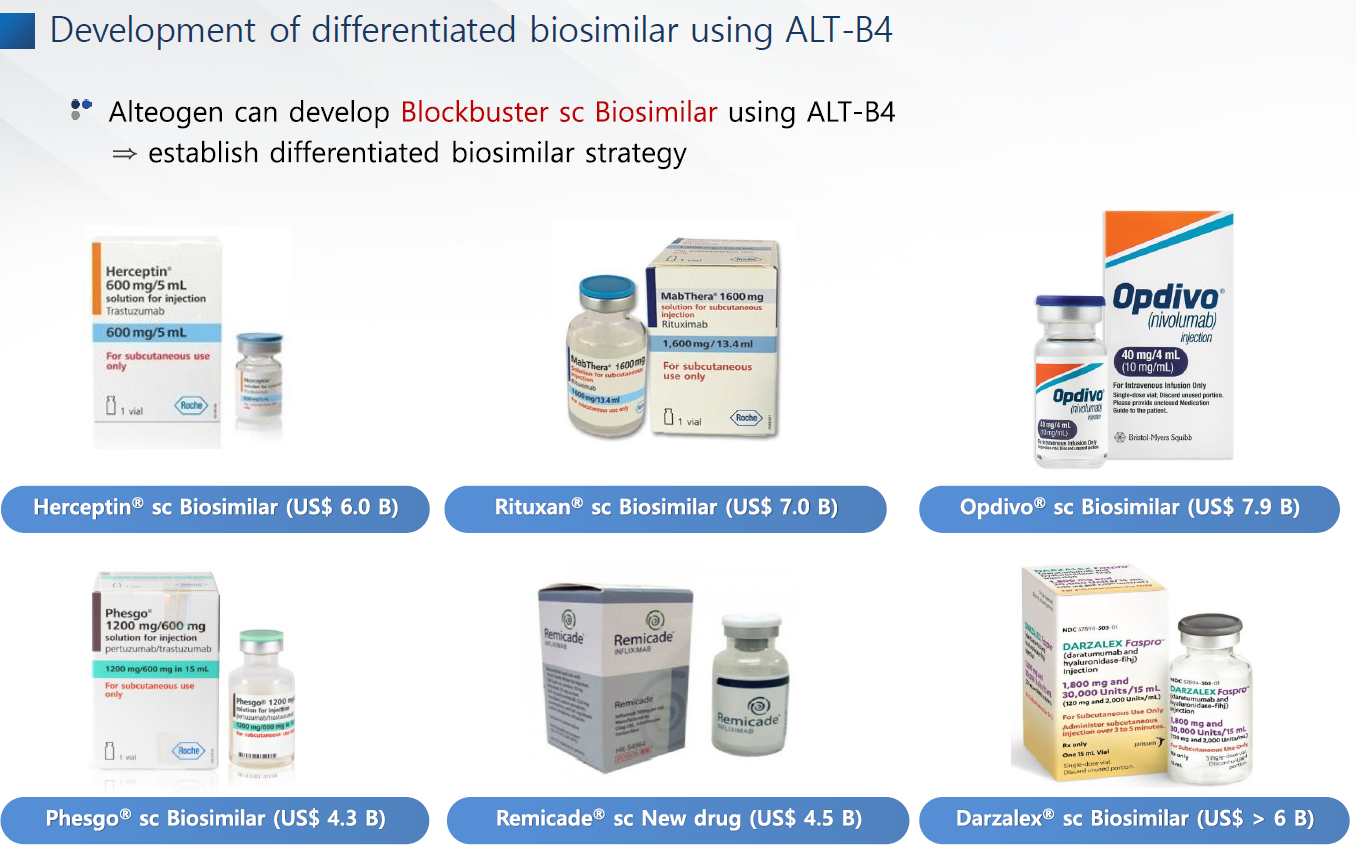
그리고 지역별 업체 중에서도 알테오젠를 전세계에 널리 알리기 위해서는 판권회사의 네임밸류가 중요하니 글로벌바이오업체를 고려하며, 향후 ALT-B4를 활용한 라이센싱아웃이나 ALT-B4를 통한 SC바이오시밀러 생산, 알테오젠 해외지사 설립과 같은 글로벌 바이오기업으로 도약하기 위해 필요한 포인트들과 연계지어 고려하고 있는 것으로 보인다.
알테오젠은 제40회 JP모건 헬스케어 컨퍼런스 및 바이오텍 쇼케이스(Biotech show case 2022)를 통해 다수의 주요 글로벌 제약사들과 미팅을 가질 예정이라고 6일 밝혔다.
JP모건 헬스케어 컨퍼런스와 바이오텍 쇼케이스는 오는 10일부터 13일까지(현지시간) 샌프란시스코에서 개최되며 코로나19 상황을 고려해 온라인으로 이뤄진다.
알테오젠은 이번 행사에서 글로벌 10대 제약사 4곳과 비밀유지협약(CDA) 및 물질이전계약(MTA) 체결 이후 본격적인 기술수출 계약과 관련한 협의를 진행할 계획이다. 특히 아일리아(Eylea) 바이오시밀러 ALT-L9의 마케팅 파트너 계약을 위해 글로벌 제약사들과 미팅을 가질 예정이다.
알테오젠 관계자는 “알테오젠의 달라진 위상은 자연스레 차기 품목인 아일리아 바이오시밀러에 대한 신뢰도 향상으로 이어져, 특별한 마케팅 활동 없이도 판권 계약에 대한 문의가 지속되고 있다”면서 “이번 행사에서 ALT-B4의 추가적인 기술수출은 물론이고 ALT-L9의 마케팅 파트너 계약 두 마리의 토끼를 잡겠다”고 말했다.
이어 이 관계자는 “ALT-L9의 경우, 현재 각 지역별로 판권 도입을 희망하는 업체들이 많아 보다 회사에 유리한 조건으로 계약하기 위한 저울질이 한창”이라며 “이번 행사에서 회사의 사업 방향성에 부합하는 좋은 파트너를 찾을 수 있을 것”이라고 전했다.
http://www.press9.kr/news/articleView.html?idxno=50229
알테오젠, JP모건 헬스케어 온라인 미팅 참여 - PRESS9(프레스나인)
[프레스나인] 알테오젠은 제40회 JP모건 헬스케어 컨퍼런스 및 바이오텍 쇼케이스(Biotech show case 2022)를 통해 다수의 주요 글로벌 제약사들과 미팅을 가질 예정이라고 6일 밝혔다.JP모건 헬스케어
www.press9.kr
'주식 > 알테오젠' 카테고리의 다른 글
| 알테오젠, ALT-B5 개발임상 노하우 이전받았다 (0) | 2022.01.13 |
|---|---|
| 알테오젠, 키트루다SC 임상 3상 시료 생산의 의미는? (0) | 2022.01.08 |
| 알테오젠, ALT-Q5 미국특허 등록 (0) | 2021.12.22 |
| 알테오젠, 삼성증권 리포트 리뷰 (0) | 2021.12.17 |
| 알테오젠, ALT-L9 내년에 글로벌임상3상 간다! (0) | 2021.12.08 |