더벨이 분석한 공시 자료에 따르면 알테오젠은 2008년 5월 설립 이래 123만 8700주의 주식선택권을 임직원에 부여했다. 올해 상반기 기준 전체 주식의 8.21%정도다. 총 201명에 스톡옵션을 지급했는데 현재 직원수가 91명이라는 점을 고려하면 중복으로 옵션을 받은 이가 적지 않다.
알테오젠 스톡옵션의 잔여 미행사 잔량은 올해 6월 말 기준으로 41만9700주였다. 전체 주식수의 3% 정도다. 하지만 올해 7월 100% 무상증자 이후 잔여 옵션 수가 83만9400주로 늘어났다. 지난 7일 종가를 계산한 잔여옵션 평가금액은 1500억원이 넘는다. 임직원들의 각 회차별 행사가격을 기준으로 계산한 옵션금액이 325억원에 그치는 점을 계산하면 차익이 1200억원이 넘는 셈이다

[제약바이오 스톡옵션 해부]'5조 몸값' 알테오젠, 잔여 주식선택권 평가액 ‘1500억’
국내 최고 자본시장 미디어 thebell이 정보서비스의 새 지평을 엽니다.
www.thebell.co.kr
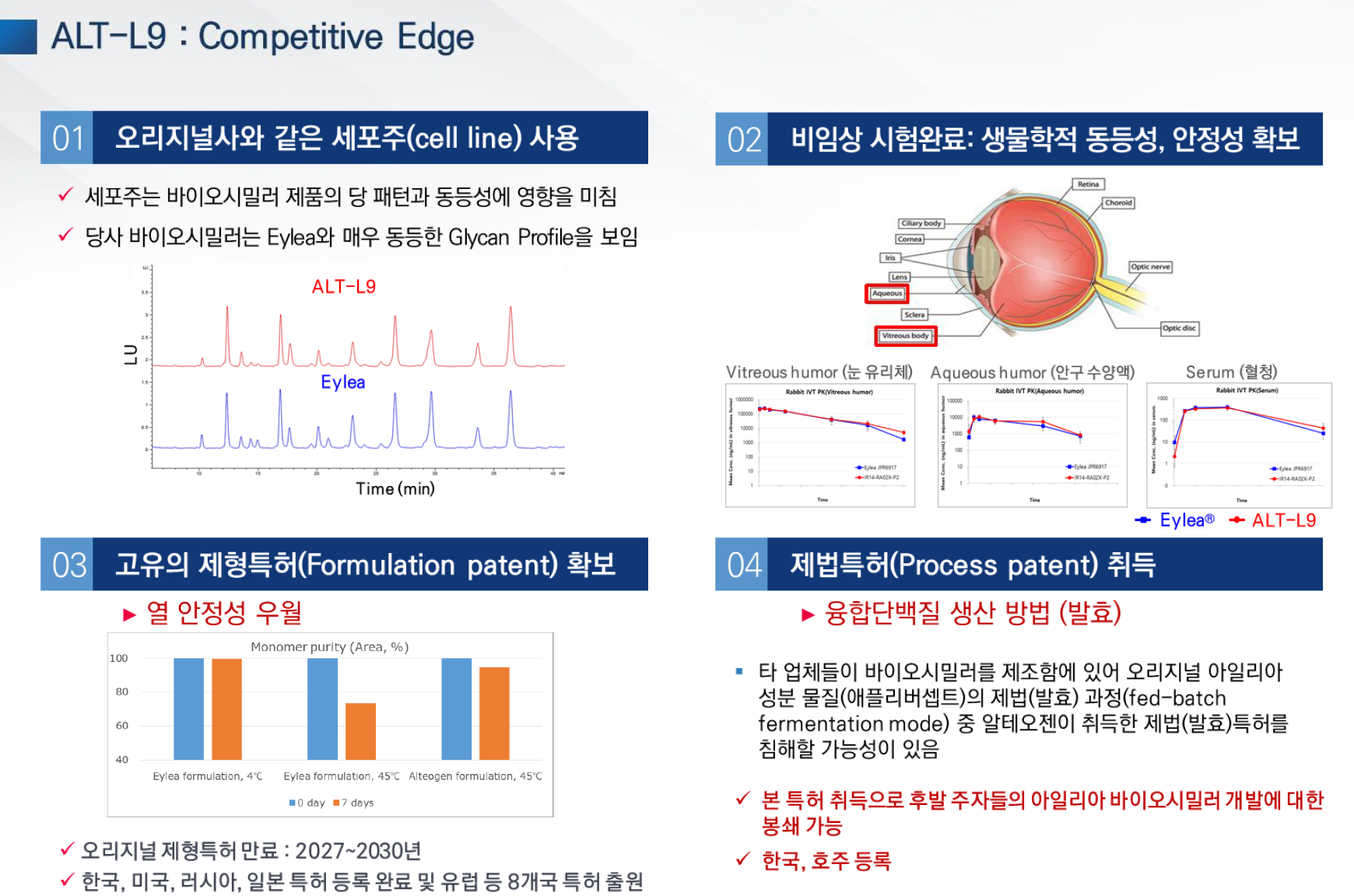
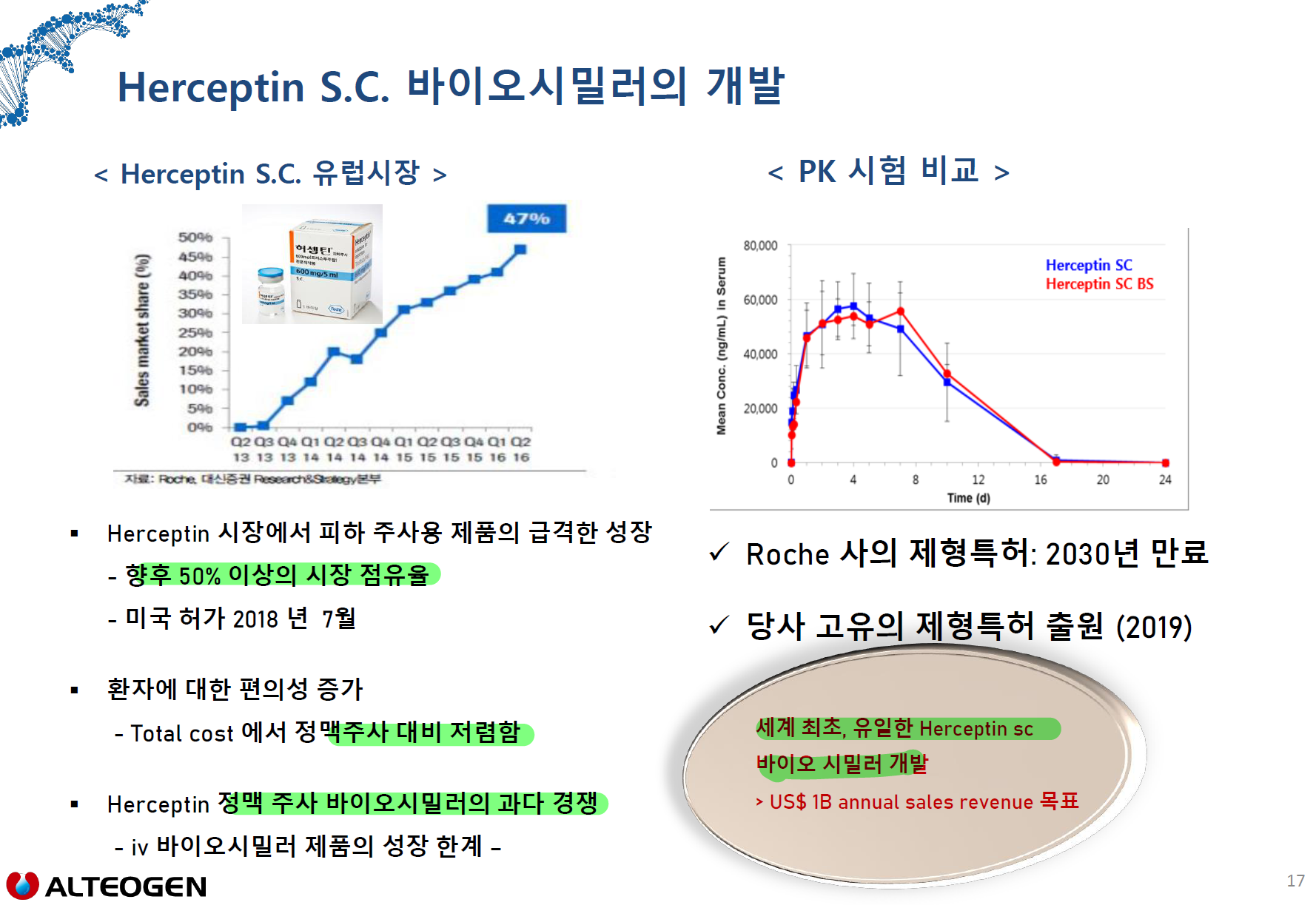
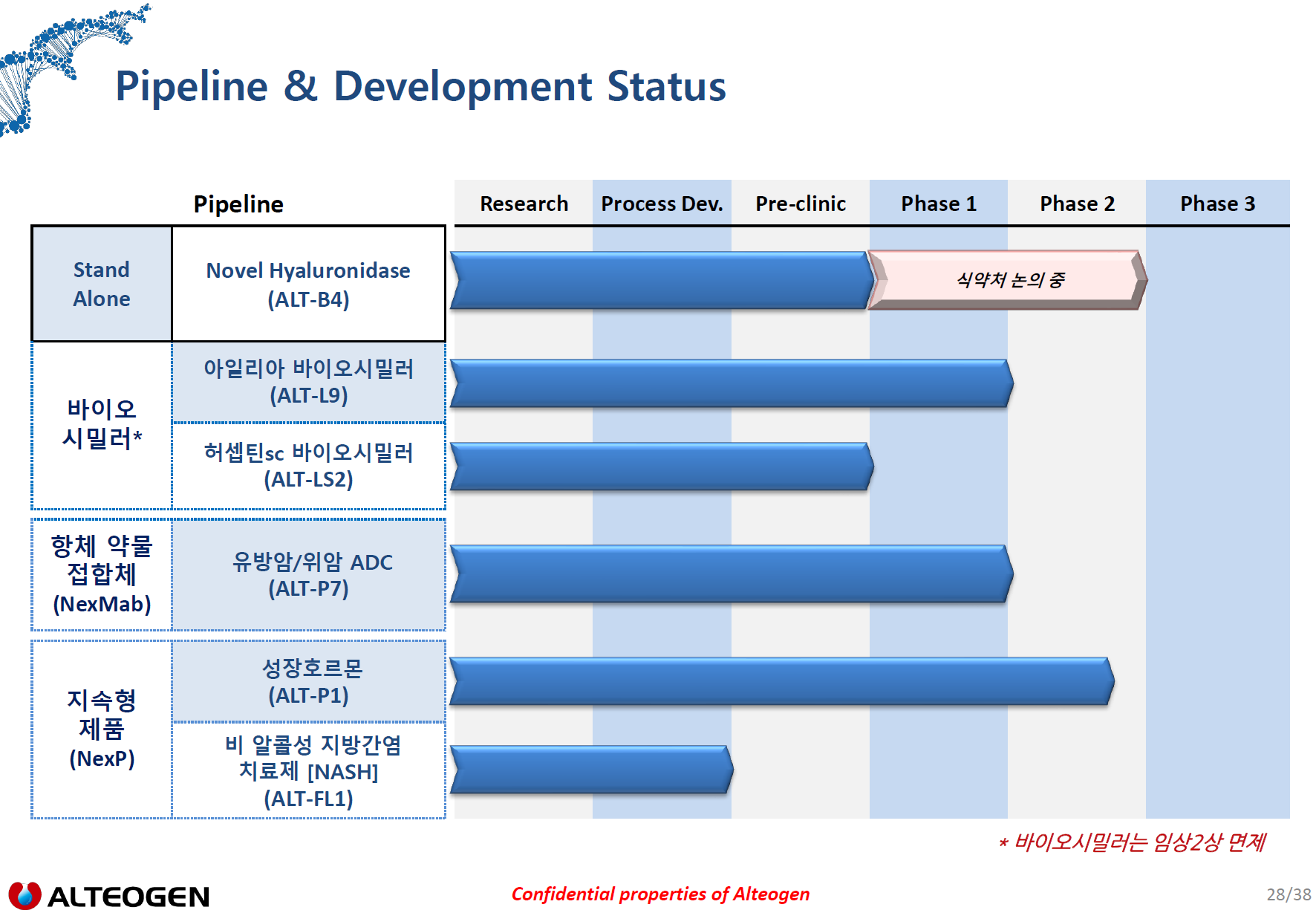
알테오젠의 ALT-B4의 대박기술수출 행진으로 시총이 5000억원에서 5조원으로 10배 가량 커지자 직원들의 스톡옵션으로 인한 가치도 엄청나다는 기사다.
스톡옵션은 기업이 임직원에게 일정 수량의 회사의 주식을 일정한 가격으로 매수할 수 있는 권리를 부여하는 제도로 전문용어로는 주식매수선택권이라고 한다. 스톡옵션은 주가가 상승하면 자사 주식을 소유한 임직원은 자신의 주식을 매각함으로써 상당한 차익금을 남길 수 있기 때문에 주로 벤처기업같은 신생 기업에서 유능한 인재를 확보하기 위한 수단이다.
알테오젠이나 최근 SK바이오팜의 사례를 보더라도 스톡옵션으로 인해 대박을 친 기사를 보면 모두의 부러움을 산다. 하지만 생각을 바꿔서 보면, 지금 알테오젠을 매수하여 미래에 글로벌 빅파마에 되었을 시점에 판다면 그것도 스톡옵션을 받은 것과 동일하다.
알테오젠을 차곡차곡 미리 매집하여 스스로 알테오젠의 스톡옵션을 받아보자.
미래 가치는 어느 정도일까? 최소 10조 이상이니 지금 사도 2배다. 그리고 셀트리온급의 덩치에 판다면 거의 10배다.
이제 올해가 3달도 남지 않았다. 최소 3건 이상의 추가 LO가 이루어질 전망이니 빨리 매집해서 셀프스톡옵션을 받자.
'주식 > 알테오젠' 카테고리의 다른 글
| 알테오젠, ALT-L9 관련 특허 일본 등록 (0) | 2020.10.22 |
|---|---|
| 알테오젠, 신규 성장호르몬 수용체 길항제 특허권 취득 (0) | 2020.10.14 |
| 알테오젠, 코리아 인베스트먼트 페스티벌 2020 참가 (0) | 2020.10.06 |
| 알테오젠, 1000억 CPS 관련 투자기관 양해각서 체결 (0) | 2020.10.05 |
| 알테오젠, 2020.09.17 IR 리뷰 (0) | 2020.09.20 |