알테오젠은 바이오텍 기업이지만, 올해는 턴어라운드 기업을 투자하는 관점에서도 좋다.
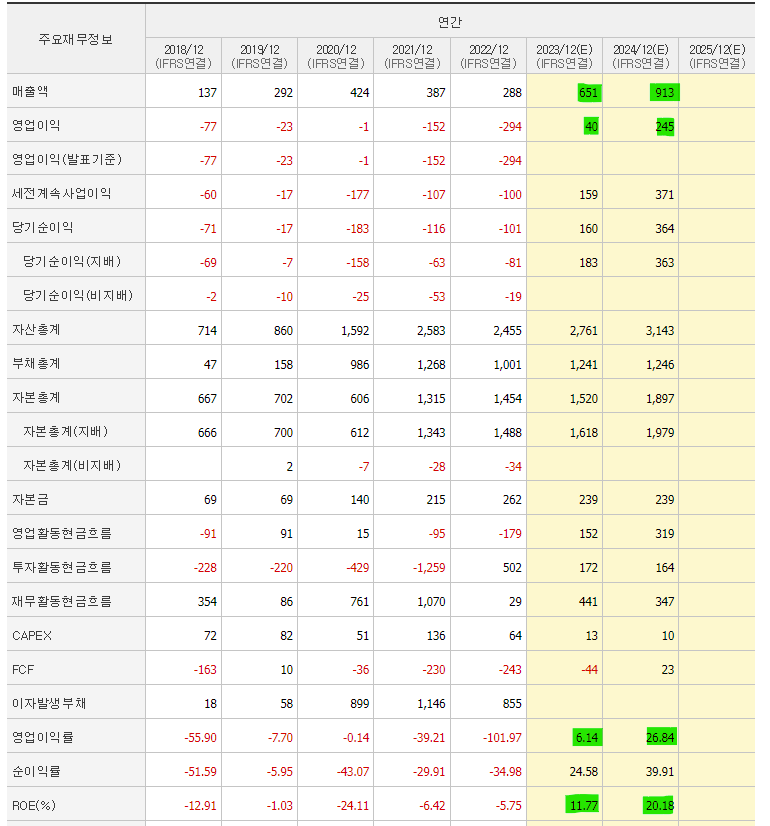
알테오젠의 올해 실적 추정치를 보면 기업 체질이 확 바뀐다.
최고매출액 달성과 영업이익 흑자전환이 예상된다.
그 이유는 머크의 키트루다SC 임상3상이 본격화되었기 때문이다. 그리고 다른 업체들의 임상이 시작될수록 매출증가와 영업이익 증가는 더 가팔라질 것이다.
알테오젠의 시간은 점점 다가오고 있다.
알테오젠이 올 상반기께 최대 수백억원대의 마일스톤을 수령할 전망이다. 정맥주사(IV)를 피하주사(SC)제형으로 바꿔주는 알테오젠의 원천기술(ALT-B4)이 사용된 글로벌 면역항암제 키트루다SC(개발사 MSD)의 임상3상 환자 투약이 본격화됐기 때문이다.
22일 관련 업계에 따르면 MSD가 추진 중인 글로벌 키트루다SC 임상3상 환자 모집이 이뤄졌으며, 최근 이들에 대한 투약이 시작됐다. 구체적인 마일스톤 규모는 확인되지 않았지만 업계는 '수백억원대 수준이 될 것'으로 전망 중이다.
MSD와의 계약 건으로 여겨지는 알테오젠의 2020년 6월 ALT-B4 기술수출 계약금은 최대 38억7000만달러(약 4조9000억원) 규모다. 당시 양사는 물질들의 개발 단계, 임상 진입과 출시 시기, 출시 이후 매출 및 누적 매출에 따라 마일스톤을 받는 형태로 계약을 체결한 것으로 알려졌다.
알테오젠이 이미 수령한 계약금 1600만달러(약 209억원)와 임상1상 투약에 따른 마일스톤 300만달러(약 40억원)를 제외하면 향후 최대 38억5000만달러를 더 받을 수 있다.
업계 한 관계자는 "초기 임상보다 후기 임상으로 진행될수록 개발 성공 가능성이 높아지기 때문에 마일스톤 규모도 커진다"며 "통상적인 기술수출에 따른 마일스톤 규모를 볼 때 3상 마일스톤은 수백억원대 규모가 될 가능성이 크다"고 전망했다.
알테오젠이 이처럼 상반기 마일스톤 수령할 것으로 전망되면서 올해 흑자전환도 가능할 것이란 게 증권가의 시각이다. 실제 이 회사에 대한 보고서를 낸 4개 증권사는 40억원 수준의 영업이익을 창출할 것으로 전망했고, 현대차증권의 경우 1000억원이 넘는 매출액 달성과 490억원의 영업이익을 달성할 것이란 장밋빛 청사진을 제시했다.
엄민용 현대차증권 연구원은 "MSD가 알테오젠 기술로 저용량 키트루다SC 임상1상을 추가로 개시한 것이 확인됐다"며 "저용량에 대한 마일스톤까지 받게 되면 수익성 개선이 더욱 가파라질 것"이라고 추정했다.
한편 알테오젠은 마일스톤 규모와 유입 시점을 묻는 질문에 "확인해 줄 수 없다"는 원론적인 답변만 내놓았다.
https://dealsite.co.kr/articles/100908
키트루다SC 투약 시작...알테오젠 흑전 기대감↑ - 딜사이트
글로벌 임상3상 환자 투약 본격화…"수백억원대 마일스톤 수령 가능성도"
dealsite.co.kr
'주식 > 알테오젠' 카테고리의 다른 글
| 알테오젠, 바이오시밀러 SC제형은 오직 알테오젠만 가능! (0) | 2023.03.30 |
|---|---|
| 알테오젠, 글로벌 제약사들만 알테오젠의 가치를 제대로 평가하고 있다! (0) | 2023.03.27 |
| 알테오젠, 오리지널 신약을 지키려면 이젠 ALT-B4가 해답이다! (0) | 2023.03.26 |
| 알테오젠, 시간이 갈수록 머크에게 ALT-B4는 중요해지고 있다 (0) | 2023.03.19 |
| 알테오젠, 신규 이사선임으로 회계 강화 (0) | 2023.03.17 |

