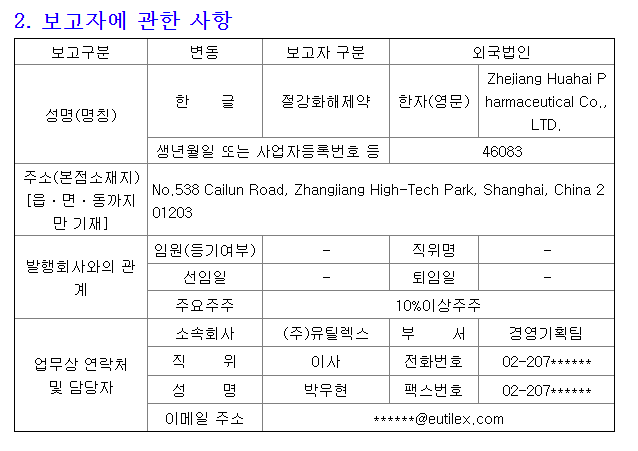
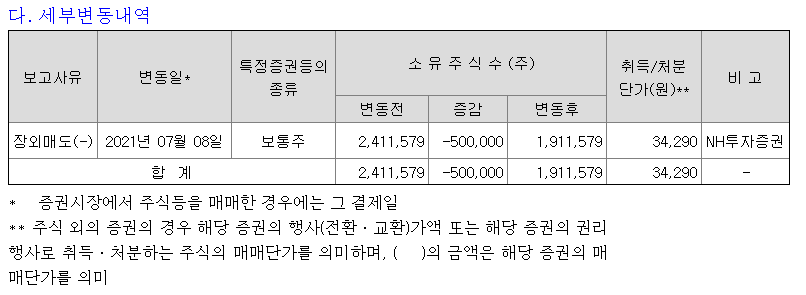
고형암 환자를 대상으로 하는 4-1BB(CD137) 면역항암제인 EU101은 미국, 한국, 중국에서 글로벌로 임상 진행중이다.
EU101의 기전은 키트루와 반대 기전으로 작용한다. 즉, EU101은 T세포의 활성을 자극시키는 역할을 하기 때문에 키트루다와 병용도 가능하다.
미국은 임상1상 첫 환자 투입이 되었고, 한국은 임상1상이 승인되어 아직 환자에게 투입되지 않은 상태다.
중국에서는 임상1상 2단계 투약이 이번에 완료되었다.
EU101은 유틸렉스의 메인 파이프라인이기 때문에 관심을 가져야 한다.
중국 협력사 절강화해제약이 진행 중인 'EU101' 중국 임상 1상의 2단계 투약이 완료됐다고 17일 밝혔다. 2017년 기술이전 이후 중국 절강화해제약은 고형암 환자 18명을 대상으로 임상 1상을 진행 중이다.
이번 임상은 단계별로 면역항암제 EU101의 용량을 늘려 투약 안전성을 확인하는 방식이다. 현재 2단계까지 투약한 6명의 환자들에게서 어떠한 이상반응도 나오지 않았다는 설명이다. 기존 용량에서 3배 이상 증량한 3단계 용량 투약은 내달부터 진행할 예정이다.
최수영 유틸렉스 대표는 "EU101의 한국 미국 중국 3개국 임상 중에서도 중국 임상이 가장 앞서고 있어, 회사에서도 관심 있게 살피고 있다"며 "최근 화해제약의 주식 일부 매각이 중국 임상에 문제가 생겼기 때문이 아닌가 하는 우려가 있었는데, 임상 순항 소식으로 주주분들의 걱정을 덜어드릴 수 있게 됐다"고 말했다.
이어 "현재 3개국 임상이 순조롭게 진행되고 있는 만큼, 조속한 시일 내에 유효한 데이터를 확보하기 위해 최선을 다할 것"이라고 했다.
유틸렉스는 2017년 EU101의 중국 개발권 및 판권을 절강화해제약에 기술이전했다. 중국에서 진행되는 EU101의 1상은 상하이의 대형 병원 2곳에서 진행 중이다.
https://www.hankyung.com/it/article/202108179104i
유틸렉스 "면역항암제 EU101, 中 1상 2단계 투약완료"
유틸렉스 "면역항암제 EU101, 中 1상 2단계 투약완료", 내달 초 3단계 진입 예정
www.hankyung.com
'주식 > 기업' 카테고리의 다른 글
| #효성첨단소재, 국내유일 탄소섬유 생산업체 (0) | 2021.08.21 |
|---|---|
| #테고사이언스, TPX-115와 CDMO가 핵심미래성장동력 (0) | 2021.08.20 |
| #이오플로우, 2022년부터 매출 본격화 기대 Feat. SK증권 (0) | 2021.08.16 |
| #테고사이언스, CDMO 계약임박은 NO, 협의중은 Yes (0) | 2021.08.15 |
| #유틸렉스, 앱비앤티셀 국내 추가 임상 신청 (0) | 2021.08.03 |