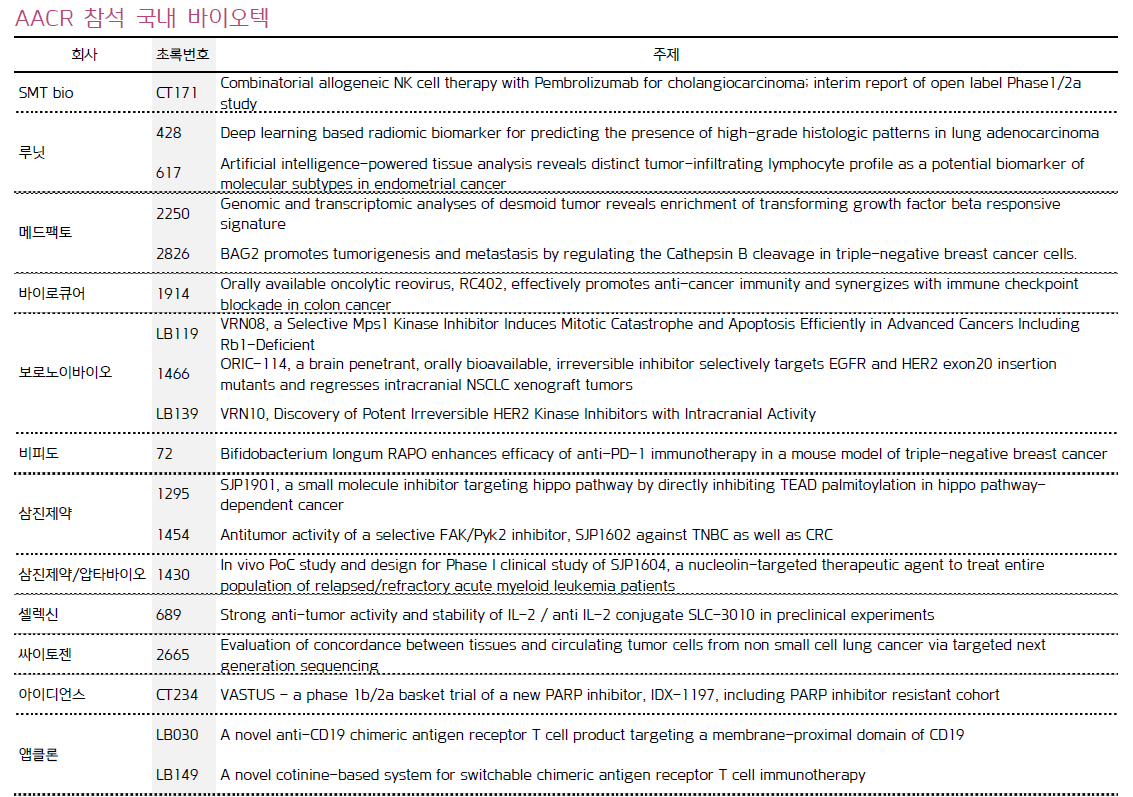
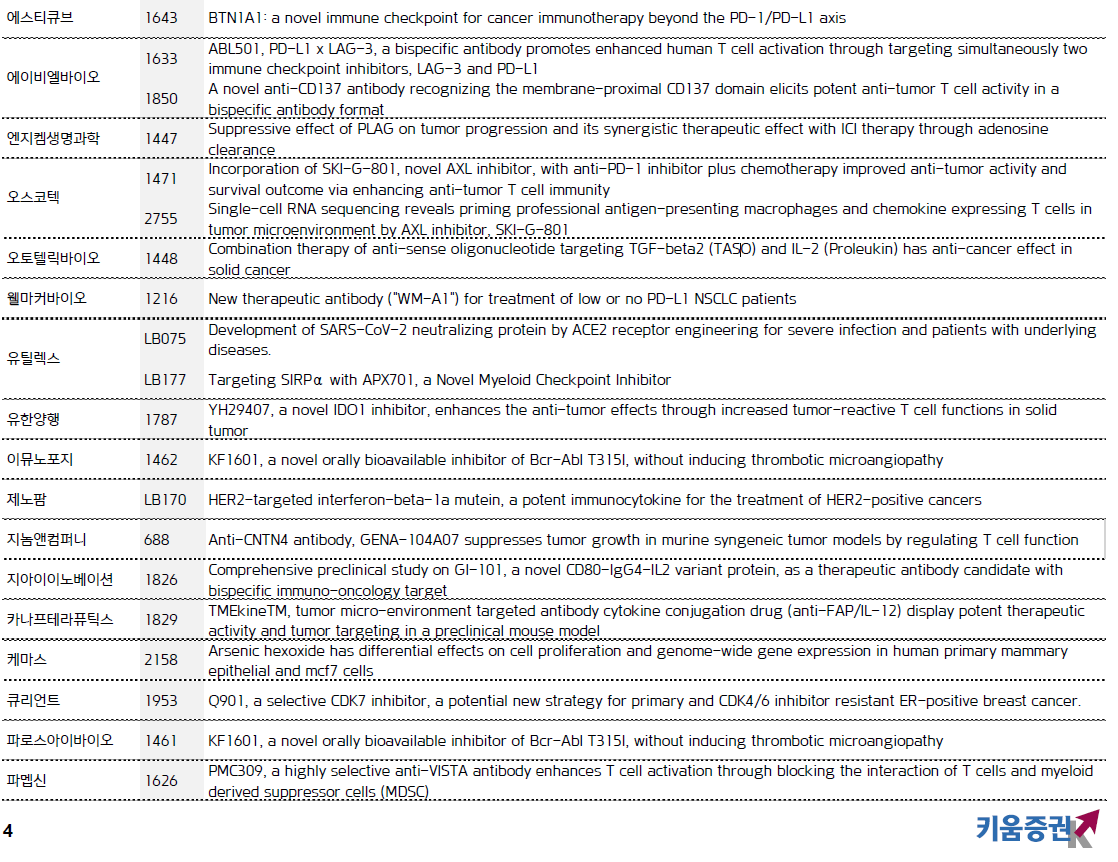
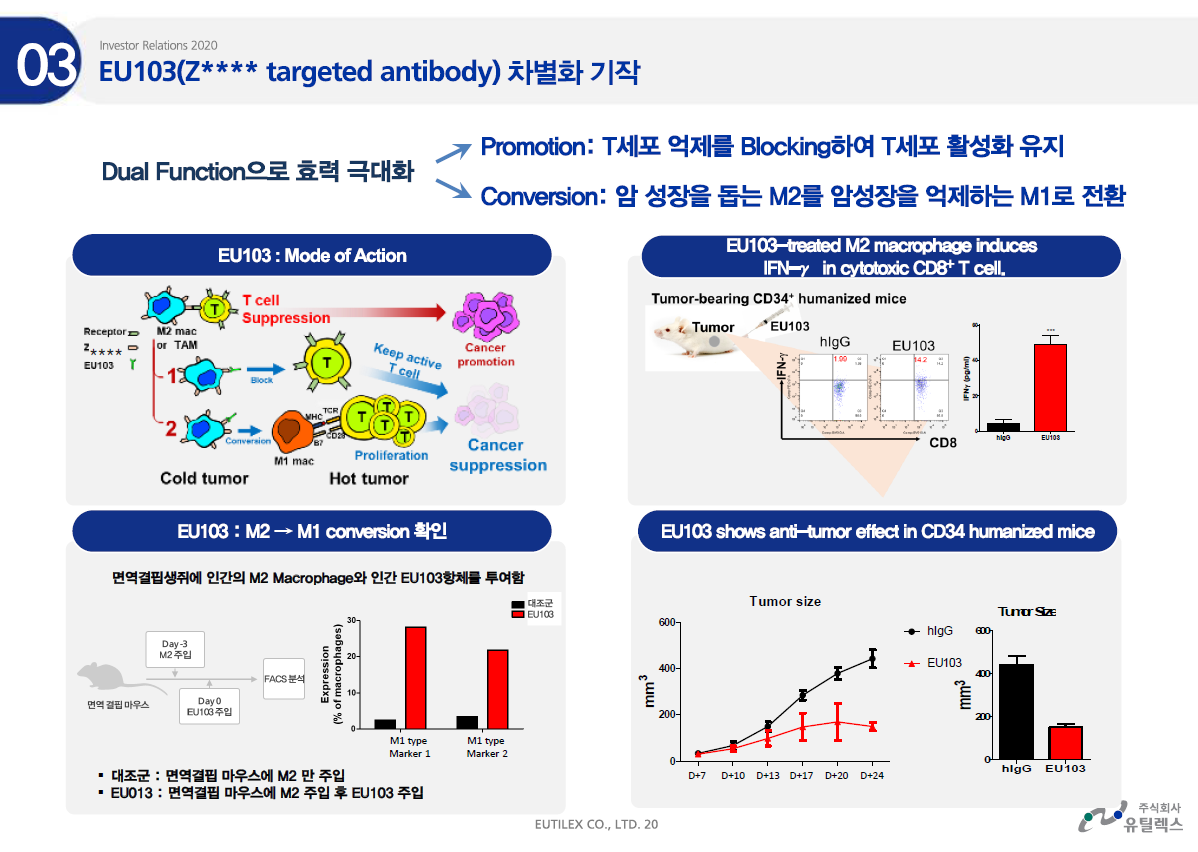
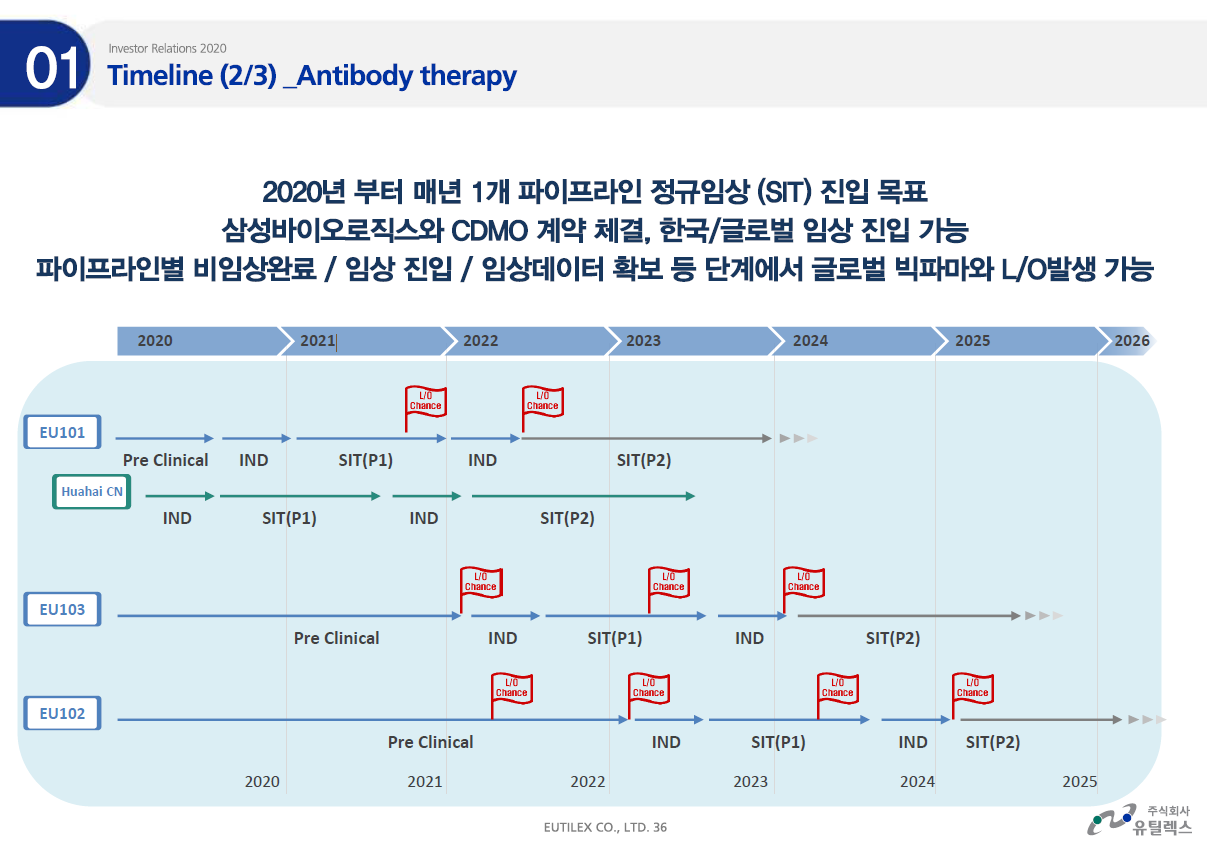
면역항암제 기업 유틸렉스가 HLA-DR 에 결합하는 키메라 항원 수용체 및 CAR-T 세포에 대한 특허가 미국에 등록되었다.
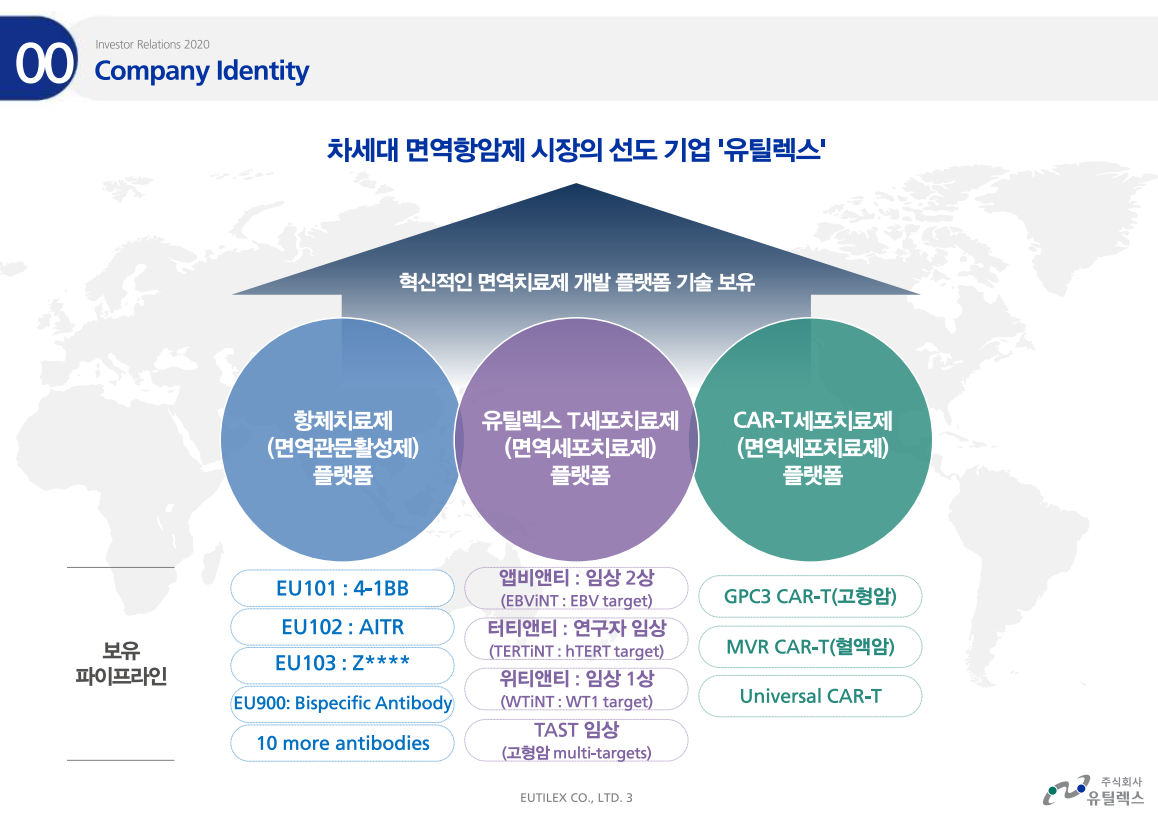
이 특허는 종양에서 과발현하는 HLA-DR을 타깃으로 하는 MVR CAR-T 세포치료제에 관한 것이다.
기존 CD19 CAR-T 세포치료제는 종양세포 뿐만 아니라 정상 B세포도 제거하며 사이토카인 폭풍으로 부작용을 유발하는 단점이 있었다. 하지만 유틸렉스의 MVR CAR-T 세포치료제는 종양세포만을 공격하며, 사이토카인 부작용도 적다.
기존 CD19 CAR-T 세포치료제의 단점만을 없앤 것이기 때문에 실제 개발에 성공하여 상용화할 경우 상당한 파급력이 있을 것이라고 생각된다.
기타 경영사항(특허권 취득)(자율공시)
| 1. 특허명칭 | HLA-DR 에 결합하는 키메라 항원 수용체 및 CAR-T 세포 (Chimeric Antigen Receptor That Binds HLA-DR and CAR-T Cell) |
| 2. 특허 주요내용 | 본 발명은 HLA-DR에 결합하는 키메라 항원 수용체 및 CAR-T 세포에 관한 것이다. 본 발명의 구체적인 내용은 서열번호 1로 표시되는 아미노산 서열을 포함하는 중쇄 상보성 결정 영역 1(HCDR1), 서열번호 2로 표시되는 아미노산 서열을 포함하는 HCDR2, 및 서열번호 3으로 표시되는 아미노산 서열을 포함하는 HCDR3를 포함하는 중쇄 가변 영역, 및 서열번호 4로 표시되는 아미노산 서열을 포함하는 경쇄 상보성 결정 영역 1(LCDR1), 서열번호 5로 표시되는 아미노산 서열을 포함하는 LCDR2, 및 서열번호 6으로 표시되는 아미노산 서열을 포함하는 LCDR3를 포함하는 경쇄 가변 영역을 포함하는, 항원 결합 분자로 상기 항원 결합 분자는 T 세포 수용체 (T cell receptor; TCR)인, 항원 결합 분자 및 이를 발현하는 세포주에 관한 것이다. 본 발명은 MVR 항체의 서열 변이를 통해 항원에 대해 다양한 결합친화도를 가지도록 설계된 특허이며, 항체 자체를 치료제로 이용하거나 항체를 이용한 치료제 (CAR-T 세포치료제) 등에 적용될 수 있을 것으로 기대한다. |
| 3. 특허권자 | ㈜유틸렉스 |
| 4. 특허취득일자 | 2021-04-19 |
| 5. 특허 활용계획 | 특허기술의 사업화와 글로벌 특허 포트폴리오 구축을 통한 기술경쟁력 강화 |
| 6. 확인일자 | 2021-04-19 |
| 7. 기타 투자판단에 참고할 사항 | -상기 등록특허는 미국 특허임 -미국 특허출원번호: 16/715,462 - 이번 미국 특허등록은 신속심사로 출원되었으며, 특허심사 하이웨이를 통해 빠르게 주요 국가에서 특허 등록될 예정임 |
'주식 > 기업' 카테고리의 다른 글
| #박셀바이오, 중앙연구소 2023년까지 준공 예정 (0) | 2021.04.26 |
|---|---|
| #유틸렉스, 차세대 파이프라인 EU505 CDMO 계약 체결 (0) | 2021.04.23 |
| #이오플로우, 진정한 목표는 세계최초 웨어러블 인공췌장 솔루션 개발 (0) | 2021.04.19 |
| #유틸렉스, 가장 기대되는 면역관문활성제 EU101->빠르면 올해 3분기 유효성 입증 (0) | 2021.04.17 |
| #인텍플러스, 인텔의 파운드리 산업 진출-> 매출 증대 기대 (0) | 2021.04.08 |